一、实验目的
1.熟悉邻菲啰啉分光光度法测定铁含量的原理和方法。
2.掌握721型分光光度计的使用方法。
二、实验原理
根据朗伯-比尔定律,当单色光通过一定厚度(l)的有色物质溶液时,有色物质对光的吸收程度(用吸光度A表示)与有色物质的浓度(c)成正比。
A=k·c·l
其中,k是吸光系数,它是各种有色物质在一定波长下的特征常数。在分光光度法中,当条件一定时,k、l均为常数,此时,上式可写成:
A=K·c
因此,一定条件下只要测出各不同浓度的吸光度值,以浓度为横坐标,吸光度为纵坐标即可绘制标准曲线。
在同样条件下,测定待测溶液的吸光度,然后从标准曲线查出其浓度。
邻菲啰啉(邻二氮杂菲)是目前分光光度法测定铁含量的较好试剂。在pH=2~9的溶液中试剂与Fe2+生成稳定的红色配合物。该反应中铁必须是亚铁状态,因此,在显色前要加入还原剂,如盐酸羟胺翳学教育网搜集整理。反应如下:
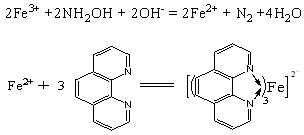
红色配合物的最大吸收波长(λmax)为508nm.
三、仪器与药品
仪器:721型分光光度计、容量瓶(50mL)、刻度吸量管。
药品:邻菲啰啉(8mmol/L,新鲜配制)、盐酸羟胺(1.5mol/L,临时配制)、NaAc(1mol/L)。
标准铁溶液(2.000mmol/L):准确称取0.7842克(NH4)2Fe(SO4)2·6H2O置于烧杯中,加入6mol/LHCl120mL和少量蒸馏水,溶解后转入1000mL容量瓶中,加蒸馏水稀释至刻度,摇匀备用。
四、操作步骤
1.标准溶液和待测溶液的配制
取50mL容量瓶7个,按下表所列的量,用吸量管取各种溶液加入容量瓶中,加蒸馏水稀释至刻度,摇匀。即配成以系列标准溶液及待测溶液。
标准溶液及待测溶液
| 容量瓶编号 |
1(空白) |
2 |
3 |
4 |
5 |
6 |
7水样(10mL) |
| 标准铁溶液 (mL) |
0 |
0.40 |
0.80 |
1.20 |
1.60 |
2.00 |
--- |
| 盐酸羟胺 (mL) |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
1.0 |
| 邻菲啰啉 (mL) |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
| 醋酸钠溶液 (mL) |
5.0 |
5.0 |
5.0 |
5.0 |
5.0 |
5.0 |
5.0 |
2.吸光度的测定
按721型分光光度计的使用方法(详见几种仪器的使用方法)选择波长λ=508nm,用空白溶液调整仪器,然后测出所配一系列溶液的吸光度,记录结果。
3.绘制标准曲线
标准曲线中Fe2+离子浓度(μmol/L)为横坐标,以吸光度(A)为纵坐标绘制标准曲线。
4.待测水样中Fe2+离子浓度的测定
根据所测得的水样的吸光度,即可从标准曲线上查得其浓度。
五、实验前准备的问题
1.为什么要控制被测液的吸光度最好在0.15~0.7的范围内?如何控制?
2.由工作曲线查出的待测铁离子的浓度是否是原始待测液中铁离子的浓度?