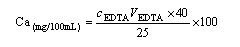一、实验目的
⑴了解牛奶酸度和钙含量的检测方法及其表示。
⑵了解配位滴定法的原理及方法。
二、实验内容
1.酸度的测定
⑴实验原理
通过测定牛奶的酸度即可确定牛乳的新鲜程度,同时可反映出乳质的实际状况。
乳的酸度一般以中和100mL牛乳0.1mol·L-1氢氧化钠溶液的毫升数来表示,正常牛乳的酸度随乳牛的品种、饲料、泌乳期的不同而略有差异,但一般均在14~18°T之间。如果牛乳放置时间过长,因细菌繁殖而致使牛乳酸度降低。因此牛乳的酸度是反映乳质量的一项重要指标。
⑵试剂及仪器
试剂:1%酚酞指示剂,0.1mol·L-1氢氧化钠标准溶液,pH=6.88标准缓冲溶液。
仪器:量筒、锥形瓶、碱式滴定管、pHS-25型酸度计。
⑶测定方法
①滴定法
量取50mL鲜乳,注入250mL锥形瓶中,用50mL中性蒸馏水稀释,加入1%酚酞指示剂5滴,混匀。用0.1mol·L-1氢氧化钠标准溶液(如何标定?)滴定,不断摇动,直至微红色在1min内不消失为止。计算酸度以100mL牛乳消耗的NaOH克数表示,或量取250mL酸牛乳,充分搅拌均匀,然后准确称取此酸牛乳15~20g于250mL锥形瓶中,加入50mL热至40℃的蒸馏水(摇匀),加0.1%酚酞指示剂3滴,用0.1mol·L-1NaOH标准溶液滴至微红色在30s内不消失,即为终点,重复三次,计算酸度(以100g酸牛奶消耗的NaOH的克数表示)。
②酸度计法
按照pH计的使用说明用标准缓冲溶液pH=6.88定位,用蒸馏水洗净电极,擦干。取50mL鲜牛奶放入100mL烧杯中,在酸度计上测定pH值。
2.钙含量的测定
⑴实验原理
测定牛奶中的钙采取配位滴定法,用二乙胺四乙酸二钠盐(EDTA)溶液滴定牛奶中的钙。用EDTA测定钙,一般在pH=12~13的碱性溶液中,以钙试剂(络蓝黑R)为指示剂,计量点前钙与钙试剂形成粉红配合物,当用EDTA溶液滴定至计量点时,游离出指示剂,溶液呈现蓝色。
滴定时Fe、Al干扰时用三乙醇胺掩蔽。
⑵试剂及仪器
试剂:EDTA标准溶液(0.02mol·L-1)、NaOH(20%)、铬蓝黑R(0.5%)或MgY-EBT作指示剂。
仪器:移液管(25mL)、锥形瓶(250mL)、滴定管。
⑶实验步骤
⑴EDTA溶液的标定(用标准锌溶液标定)
⑵钙含量的测定
准确移取牛奶试样25.00mL三份分别加入250mL锥形瓶中,加入蒸馏水25mL,加入2mL20%NaOH溶液,摇匀、再加入10~15滴铬蓝黑R指示剂,用标准EDTA滴定至溶液由粉红色至明显灰蓝色,即为终点,平行测定三次,计算牛奶中的含钙量,以每100mL牛奶含钙的毫克数表示。将纯鲜牛奶换成高钙牛奶,重复做三次,计算高钙牛奶中的含钙量。